关于注射剂一致性评价,从2015年《国务院关于改革药品医疗器械审评审批制度的意见》初次提出,到2017年国家局发布了《关于鼓励药品医疗器械创新实施药品医疗器械全生命周期管理的相关政策》征求意见稿,再次单条列出,这项工作的推进已成了板上钉钉的事。
错过了“口服固体制剂一致性评价”先机,见识了国家局的认真气力,尝到了通过一致性评价后的优厚福利,药企们哪里会放过这一强烈的信号,坚定步伐走在政策前。
从今年4月份至今,
就站出来8个率先申请一致性评价的注射剂。
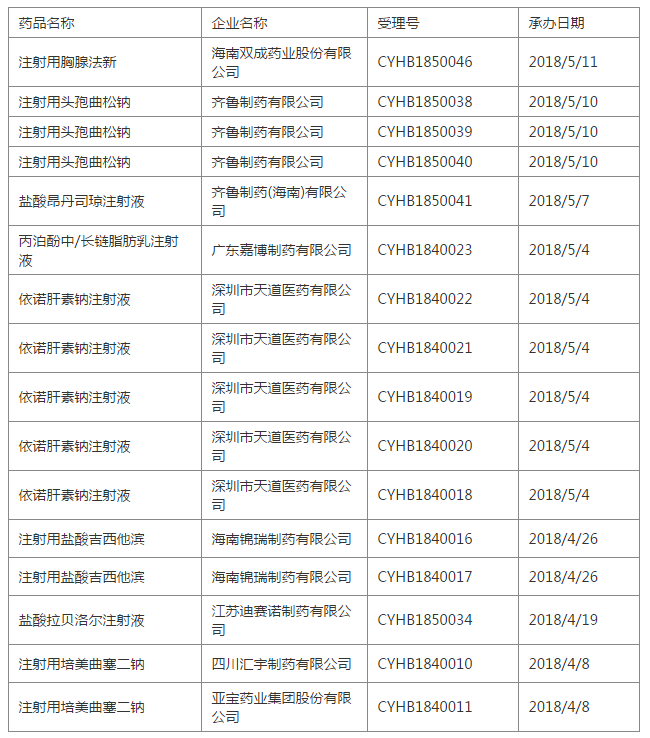
这一波申报来得“没有一点点防备”。
关于注射剂一致性评价的操作方法,最新的文件还停留在2017年12月药品审评中心发布的《已上市化学仿制药(注射剂)一致性评价技术要求(征求意见稿)》。
技术要求意见稿只提到“参考FDA或者EMA的指导原则对特殊注射剂品种(如脂质体、静脉乳、微球、混悬型注射剂等) 开展与参比制剂的对比研究”,并无一般性的指导原则。
弱弱问了一句:那到底是做生物等效性试验(BE),
还是做临床有效性试验?
带着一脸疑问,搜索药物BE备案信息,结果出人意料,还!真!有!而且是最近才公示的备案。
从5月份开始,注射剂BE试验陆续有备案,品种有:左亚叶酸钠注射液、氟比洛芬酯注射液、重组人促卵泡激素注射液、丙泊酚中/长链脂肪乳注射液。
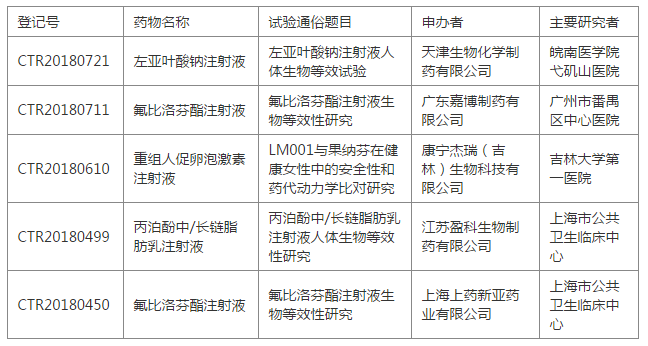
从拟招募的受试者例数:16,24,32,34例,到主要终点指标:主要药代动力学参数T max 、C max 、AUC 0-t 、AUC 0-∞ 、λ z 、t 1/2 、V d 、CL,与口服固体制剂的BE试验基本一致。
哪里不对?对于静脉注射给药,直接入血,不存在生物利用度和吸收的问题啊。这是什么操作?
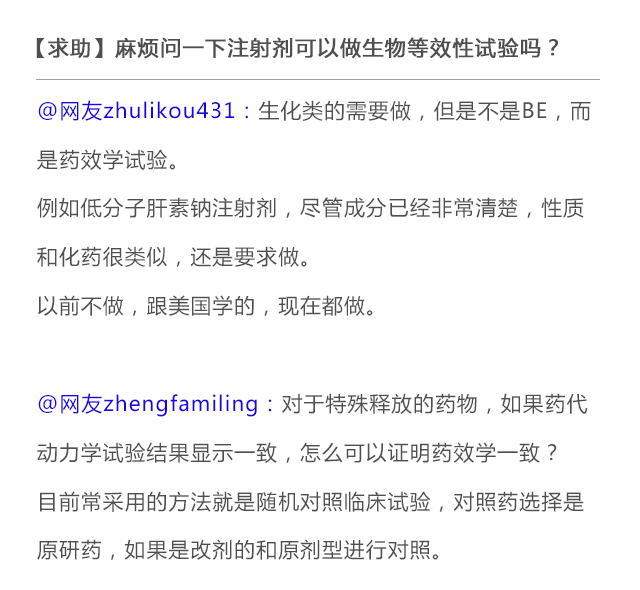
关于注射剂做不做生物等效性试验的问题,
业内网友也众说纷纭。


最后,我们看看第一个表格“申请注射剂一致性评价”的品种,有没有做生物等效性试验呢?
答案是:并没有。
那么,在默默等待国家局发布注射剂一致性评价的技术指南正式稿之际,你有什么建议呢?



