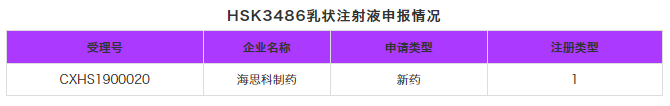
上周,有3个重磅仿制药评审情况有了新的进展,分别是:阿伐那非、右兰索拉唑肠溶胶囊和氢溴酸替格列汀片。此外,HSK3486乳状注射液以新药形式申报,也进入了药品评审中心的审评序列。
阿伐那非片:由Vivus公司生产,与伟哥和希爱力属于同一类药品。这些药物均属于5型磷酸二酯酶抑制剂(PDE5-I),通过增加流向阴茎的血流起作用。于2012年4月27日获得美国食品与药物管理局(FDA)批准,目前已在美国、德国、法国等多国上市,欧美主要国家销售额约为$4,045万,该品种在国内尚无生产和进口。
临床结果显示,阿伐那非可持久有效安全地用于治疗勃起功能障碍,且对 1 型和 2 型糖尿病勃起功能障碍患者及已施行前列腺切除术的勃起功能障碍患者均有效。
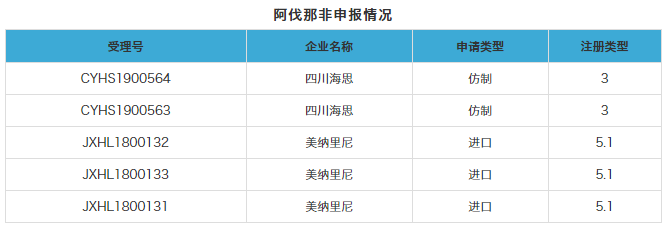
企业申报情况:目前,阿伐那非片除美纳里尼以进口药的方式申报外;还有四川海思制药以新注册分类3类申报上市,已被CDE成功受理。若四川海思的阿伐那非片成功通过审评,将成为该品种的首仿,市场潜力巨大。
右兰索拉唑肠溶胶囊:由武田制药(Takeda)研发,为质子泵抑制剂(PPI),特异性作用于胃壁细胞上的H+/K+-ATP酶,抑制胃酸分泌,主要是通过作用于具体的质子泵,而阻碍胃酸产生的最后一步。该药可用于治疗所有等级的糜烂性食管炎(EE),维持EE的愈合,缓解胃灼热,并可用于治疗非糜烂性胃食管反流病(GERD)相关的胃灼热症状。
右兰索拉唑肠溶胶囊于2009年1月30日获得美国食品药品管理局(FDA)批准。由武田在美国上市销售,商品名为Dexilant。目前在国内仍无首仿。
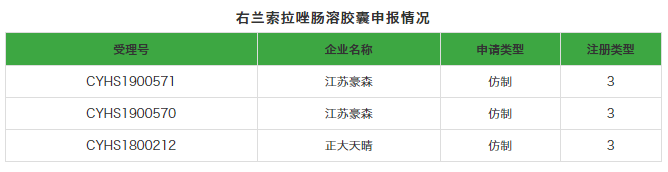
企业申报情况:右兰索拉唑肠溶胶囊在国内批文数为“0”,暂无企业在中国生产销售。目前,江苏豪森和正大天晴均以新注册分类3类申报上市。其中,江苏豪森是上周刚踏进抢占该品种的首仿行列。而无论哪家企业率先通过评审,获得首仿,也必将打开右兰索拉唑肠溶胶囊在国内上市销售的局面。
氢溴酸替格列汀片:由田边三菱制药公司研制,为二肽基肽酶-Ⅳ(DPP-4)抑制剂,用于2型糖尿病的治疗。通过抑制DPP-4的活性阻碍胰高血糖素样肽-1(GLP-1)的降解,以提高血液中GLP-1的浓度发挥降糖作用。2012年9月在日本首次上市,至今在国内仍无企业生产销售该药品。
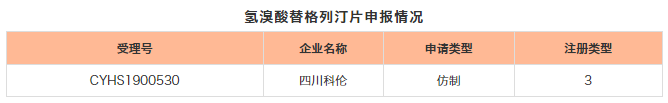
企业申报情况:目前,氢溴酸替格列汀片只有四川科伦1家企业以新注册分类3类申报。若此次科伦成功获批,上市销售,将超越由Mitsubishi Tanabe/田边三菱开发,在中国尚处于临床阶段的原研。国内,大多DPP-4抑制剂“列汀类”的药品已陆续进入国家医保行列,替格列汀作为其中一员,通过CDE评审后,将有望被纳入到医保名单,颇具市场竞争力。
※ HSK3486乳状注射液:是海思科开发的全新、具有独立知识产权的静脉麻醉药物,拟用于手术麻醉诱导、内镜诊疗的镇静/麻醉等适应症。HSK3486于 2016 年 1 月获得中国国家食品药品监督管理局的Ⅰ-Ⅲ期《药物临床试验批件》并启动临床试验。
基于未来开拓 HSK-3486 国际市场的考虑,海思科还拟在美国开展临床试验,2019年3月向美国 FDA 递交了 Pre-IND 会议申请并获得邮件确认。
企业申报情况:HSK3486乳状注射液作为国内较新推出的静脉麻醉用药品种,海思科制药经过开发创新,以新药1类的注册类型申报,目前已被CDE成功受理。
此外,由于HSK3486的适应症众多,对外科手术应用广泛,若该品种在国内成功上市,将大大丰富了海思科静脉麻醉药物的产品线。