前言
从2016年3月5日始,国务院办公厅印发《关于开展仿制药质量和疗效一致性评价的意见》国办发〔2016〕8号,明确:化学药品新注册分类实施前批准上市的仿制药,凡未按照与原研药品质量和疗效一致原则审批的,均须开展一致性评价。一致性评价进入热火朝天的实施阶段。
一致性评价一般实施环节包括“参比制剂备案/选CFDA参比目录——药学研究——BE备案——BE试验——申报受理——审评审批”,完成整个流程大约需要20~28个月。
一致性评价对于药品生产企业,既是挑战又是机遇。289目录品种、17740个批准文号或注册证号,涉及1817家国内生产企业、42家进口药品企业,优胜劣汰,如何根据药品市场信息和一致性评价动态,选择有把握的品种进行评价,至关重要!
本期分析
药春秋(ID:bryaochunqiu)根据市场反馈和调研信息,对289目录品种-阿昔洛韦片进行分析,供生产企业的小伙伴参考。
批准文号数量:
阿昔洛韦片100mg,75个;
阿昔洛韦片200mg,22个;
阿昔洛韦片400mg, 3个。
其中被列入289目录的是阿昔洛韦片200mg。
调研数据
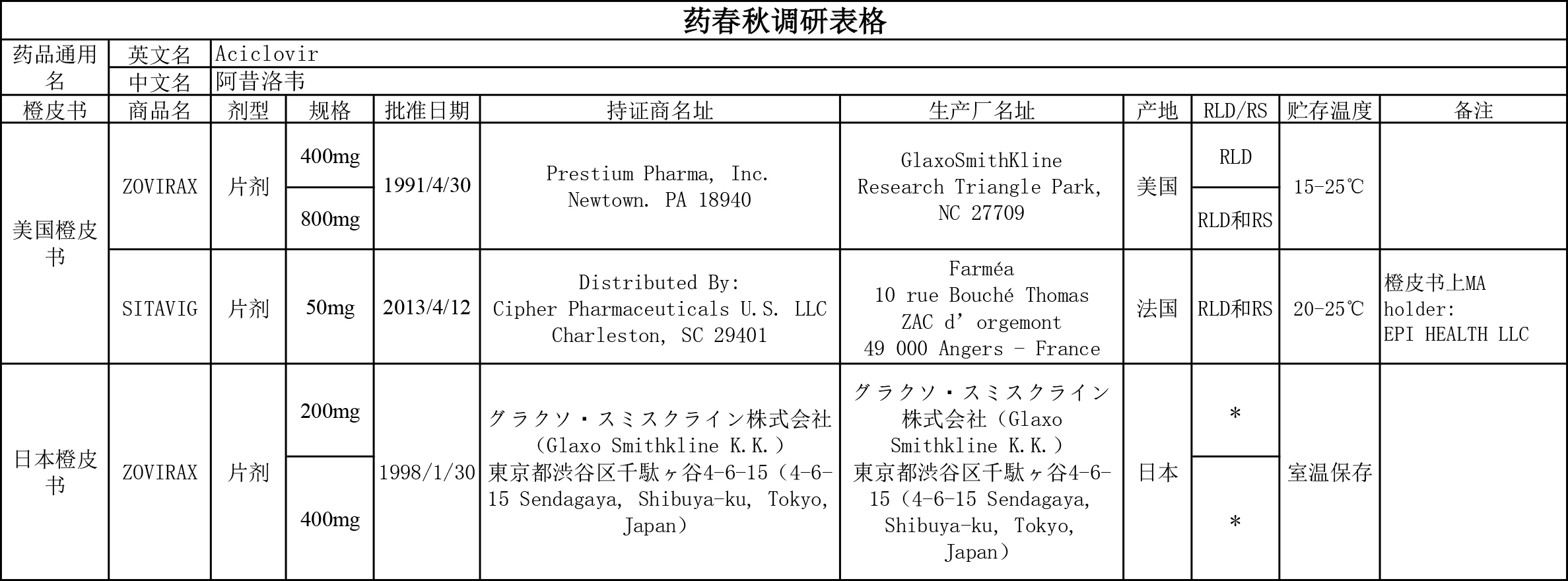
国外上市情况
阿昔洛韦片在美国、日本上市的规格是50mg、200mg、400mg和800mg。
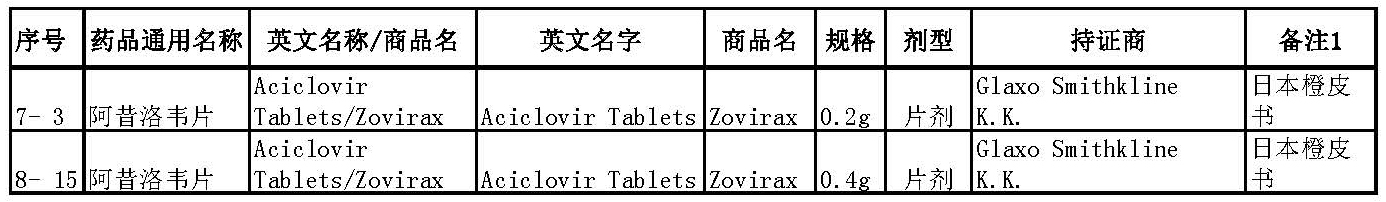
CFDA参比目录
从国外上市情况与CFDA参比制剂目录看,均无100mg的阿昔洛韦片,但在中国,阿昔洛韦片100mg的批文数量和企业参比制剂备案数远高于200mg和400mg规格。
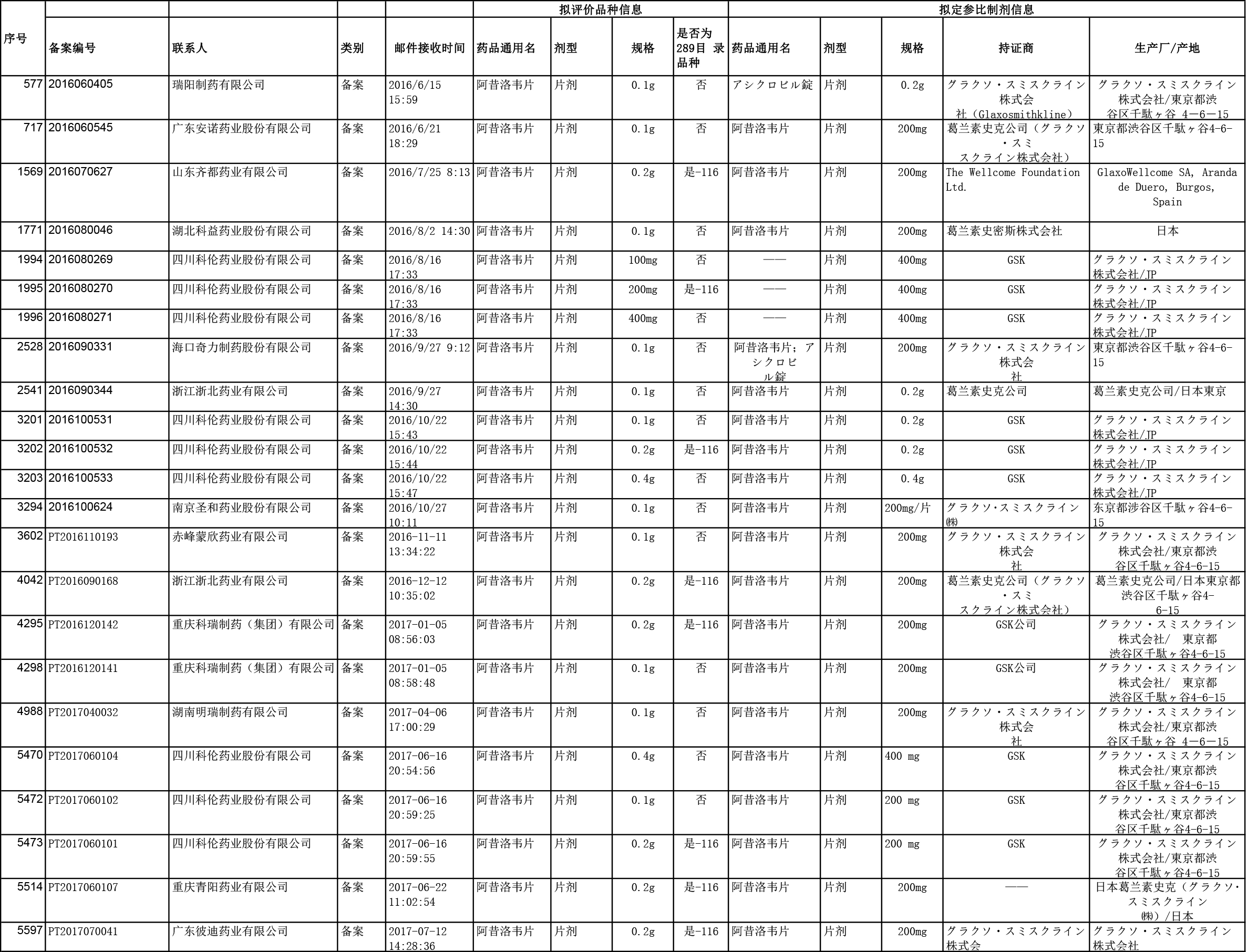
企业参比制剂备案
企业参比制剂备案统计可得:阿昔洛韦片100mg,备案数量12个;阿昔洛韦片200mg,备案数量8个;阿昔洛韦片400mg,备案数量3个;共13家企业申请备案。
企业均选择日本葛兰素史克的阿昔洛韦片200mg作为阿昔洛韦片100mg的参比制剂。
BE备案
截止11月1日,CDE临床试验登记平台暂无阿昔洛韦片的BE备案信息,也无一致性评价申报,大胆推测企业均还处于药学研究,甚至是参比制剂备案或选购阶段。
综上所述,结合给多家药企的采购经验,药春秋建议:阿昔洛韦片100mg、200mg规格的企业,可选购日本葛兰素史克200mg阿昔洛韦片作为参比制剂。
曾用阿昔洛韦作为研究对比药物的,有:万乃洛韦、伐昔洛韦、泛昔洛韦、更昔洛韦。
采购/咨询
客服 黄姑娘 18138751390
客服 林妹妹 18011892830
客服 卜才女 18011892831




