11月6日,齐鲁制药两款重磅仿制药获批上市,分别是注射用紫杉醇(白蛋白结合型)和他达拉非片。由于均按照4类注册,获批后视同通过一致性评价。这样一来,这两款重磅品种在国内通过一致性评价的仿制企业均达到3家。
01
注射用紫杉醇(白蛋白结合型)
白蛋白紫杉醇由美国Abraxis BioScience公司开发,是一种紫杉醇与白蛋白结合的全新制剂,克服了普通紫杉醇水溶性差、效率低和副作用大等缺点,于2005年1月被FDA批准上市治疗乳腺癌(商品名Abraxane),随后又获批治疗肺癌、胰腺癌。
2010年新基以29亿美元首付款收购Abraxis,将Abraxane收入囊中。2018年,Abraxane全球销售额约为10.62亿美元。
Abraxane于2008/6/10在国内获批。百济神州在2017年7月通过与Celgene交易获得了Abraxane在国内的商业权利。
齐鲁是继石药、恒瑞之后国内第3家获得该品种仿制药上市资格的企业。另外,海正、科伦和康禾生物等企业的白蛋白紫杉醇上市申请也正处于“在审评”阶段。
从中标价格中值来说,新基、石药和恒瑞分别为5510元、2680元和3280元(100mg/支)。值得注意的是,原研新基目前已经实现多次降价,在江苏、山东等地的最新中标价格为3350元(100mg/支)。
02
他达拉非片
他达拉非是一款选择性、可逆性磷酸二酯酶5(PDE5)抑制剂,原研厂家为礼来。
该药用于解决男性勃起障碍(ED)的适应症上和西地那非、伐地那非不同的地方在于他达拉非的疗效持续时间长达36小时,远长于后两者3-4小时的疗效持续时间,降低了患者在服药时间方面的顾虑。
除此之外,他达拉非还被批准用于治疗良性前列腺增生以及肺动脉高压。
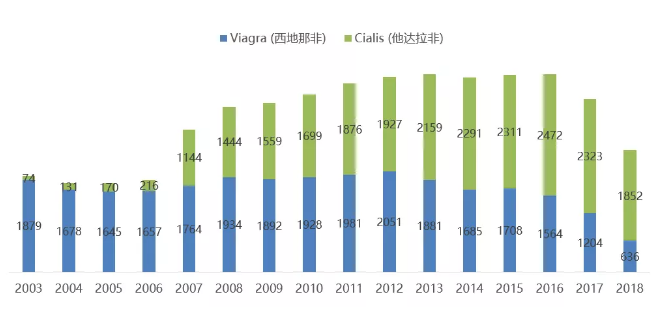
礼来在长效PDE5抑制剂基础上于2007年6月推出了每日1次5mg小剂量的口服他达拉非,革新了男性ED治疗的新模式,彻底解放了患者服药时间的束缚,这也使得他达拉非在ED药物市场的份额逐渐追平并反超了比大名鼎鼎的伟哥(西地那非)。
他达拉非原研于2004年11月在中国上市,每日1次5mg小规格则是2013年12月在中国上市,目前在国内已经失去了专利保护。齐鲁是继长春海悦、南京正大天晴之后第3家获得该品种仿制药上市资格的国内企业。
据悉,该品种除已经获批上市的3家厂家之外,还有包括恒瑞、东阳光药等在内的13家企业按照新4类申报。除此之外,还有5家企业开发口服混悬液和口腔速溶膜。



