布鲁顿酪氨酸蛋白激酶(BTK)作为B细胞受体通路的重要信号分子,在B淋巴细胞的各个发育阶段均表达,在恶性B细胞的生存及扩散中起着重要作用。
BTK抑制剂作为突破性疗法在2013年底面世,为B细胞类非霍奇金淋巴瘤患者(这类患者占到全部NHL的大约70%)提供了治愈的可能,因此上市后大受欢迎,短短5年内市场规模便已经扩张到60亿美元。
全球已有两个BTK抑制剂上市(伊布替尼、阿卡拉布替尼),其中伊布替尼作为领域第一个上市的产品,更广为人知,整个BTK抑制剂的市场几乎被伊布替尼独占,这是市场对“First in class”的回报。
伊布替尼获批的第一个适应症是套细胞淋巴瘤(MCL),阿卡替尼目前唯一获批的适应症也是MCL。
MCL通常是侵袭性的非霍奇金淋巴瘤(NHL),起源于“套区”的B细胞。2014年,美国约有70,800新增NHL病例,其中MCL新增病例为总数的 6%(约4,200起)。
在今年1月,国产的泽布替尼拿到了该适应症的FDA“突破性疗法”资格,成为了潜在的BTK抑制剂“Best in class”。
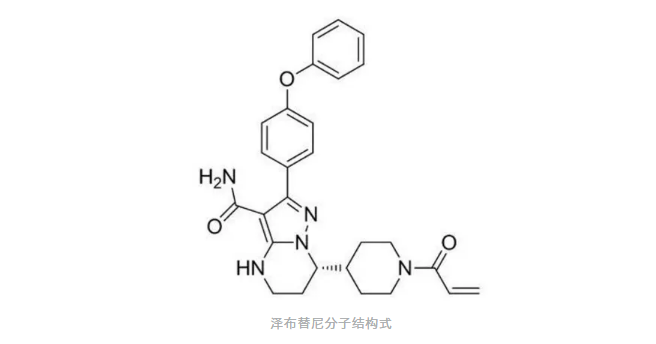
这是中国大陆首个获得FDA突破性疗法认定的新药。
近日(8.22),美国FDA受理了泽布替尼用于治疗先前至少接受过一项治疗的套细胞淋巴瘤(MCL)患者的新药上市申请(NDA)并授予优先审评资格。
泽布替尼,由百济神州自主研发的高选择性BTK抑制剂国产创新药,历时近7年开发而成,其设计旨在最大化BTK占有率、最小化脱靶效应,目前全球进行广泛的关键性临床试验项目,在多项B细胞恶性肿瘤中展现了成为新治疗方案的潜力。
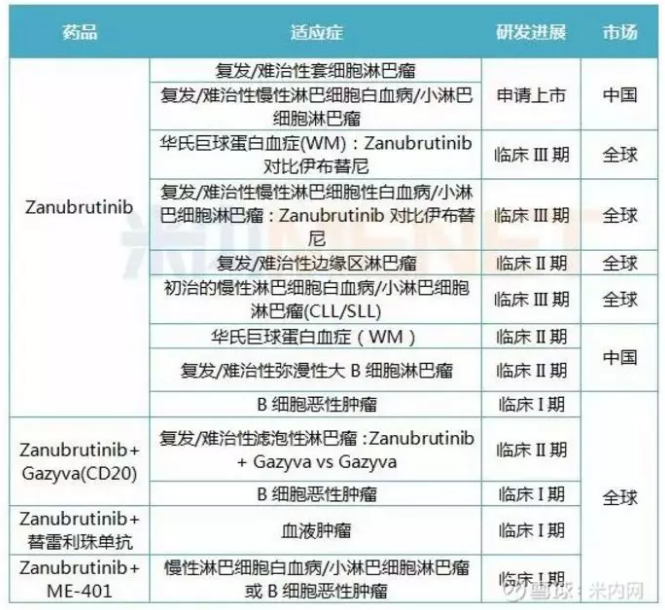
除了在美国申报,在国内百济神州也同步进行上市申请。
2018年8月和10月,百济神州分别向NMPA提交治疗复发/难治MCL和CLL的上市申请,并因“具有明显治疗优势创新药”获得优先审评资格,有望在2019年正式获批上市。
一个潜在的“Best in class”正在酝酿中。
作为后起之秀,想要站稳脚跟,必须药友更直观、更坚实的数据支持。而与市场第一位的伊布替尼开展头对头临床研究,便是获得最直观证据的有力方式,这是一次有风险的挑战,要么赢要么输。
百济神州在2017年、2018年先后启动了两项泽布替尼与伊布替尼的头对头Ⅲ期临床研究,分别针对WM(华氏巨球蛋白血症)和复发/难治型CLL(慢性淋巴细胞白血病)。这是泽布替尼开发过程中相当引人注目的一步。
前期的临床研究中,泽布替尼在这两个适应症中都体现出更具优势的数据,比如在针对WM的一项临床研究中,泽布替尼的VGPR(非常好的部分缓解)高于既往报道的伊布替尼治疗复发/难治WM所获得的VGPR率。同时,耐受性良好,毒副反应少,差距较为明显。据了解,泽布替尼针对WM的与伊布替尼的头对头临床研究正在进行中,预计将在2019年下半年公布结果
作为有望在全球第三个上市的产品,要证明自己是best-in-class,泽布替尼必须拿出一份漂亮的成绩单。
在新药研发的竞争中“没有最好,只有更好”。
国产创新药的崛起。



